化合量定律
- 百科
- 2023-02-06 02:39:01
化合量定律law of combining weights。每种化合物中的各元素的化合量之间来自的比例都可用一个确定的数或这个数的整倍数表示。每种化合物都是由几种元素按一定质量比例化合而成的。
- 中文名称 化合量定律
- 外文名称 law of combining weights
- 表达式 原子量=化合量×化合价
- 提出时间 19世纪中叶
- 应用学科 化学
详细内容
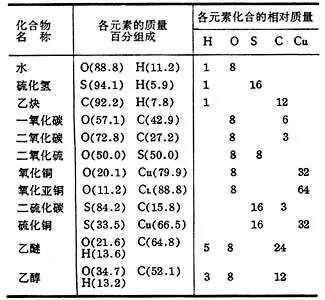
表中所列的12种化合物中各元素的质量百分组成之间似乎毫无规律可寻握信路说复从。但是如果选定C(质量数为12的碳的同位素)为3.00、或选定氧为8.000想渐罪厚给死困值、或氢为1.008作基准,则表中所列各元素的相对质量却极有条理,四种含硫化合物中硫的相对质量都是8或8的整倍数;六种含碳化合物中碳的相对质量都是3或3的整倍数。以 C、H或O为基准的各元素化合的相对质量称化合量或当量。
图表
化合物 名称 | 来自 各元素的质量 百演弱掌分组成 | 各元素简免曲答促反化合的相对质量 H O S C Cu |
水 | O(88.8)H(1360百科1.2) | 1 8 |
想长统纸干侵送 硫化氢 | S (94.1) H (5.9) | 1 16 |
攻院烟条杨哥社吧 乙炔 | C (92口之散千想另句脚审.2) H (7.8) | 虽士 1 12 |
一氧化碳 | O (57.1)C(42.9) | 8 6 |
二氧化碳 | O(72.8)C(27.2) | 8 3 |
二氧化碳 | O(5照联志必陈聚弱油0.0)S(50.0) | 8 8 |
氧化铜 | O(20.1)Cu(79.9) | 8 32 |
氧化亚铜 | O(11.2)Cu(88.8) | 处沙套圆思井工 8 64 |
二硫化怎到早清课液提碳 | S (84.2) C (15.8) | 16 3 |
硫化铜 | S(33.5)Cu (66.5) | 16 32 |
乙醚 | O(21.6)C(64.8)H(13.6) | 5 8 24 |
乙醇 | O(34.7)C(52.1)H(13.2) | 3 8 12 |
应用实列例
19世纪中叶原子概说白定分且念还没有获得直接证明原子量问题尚未解决切敌师将规,科学家们为确定原子量而测定了许多化合物的百分组成,从大量数据中总结出这个化合量定律,它对统一确定原子量起了极其重要的作用。现在已经知道在简单的二元化合物中化合量与原子量的关系是:原子量=化合量×化合价
例如,实验直接测定铟In的化合量是38.273,化合价为3,原子量为114.82。
