三氧化二磷
- 百科
- 2023-01-09 21:53:34
三氧化二磷是一种白色的有毒固体或无色液体,有蒜臭。它可溶于苯、二硫化碳等有机溶来自剂,遇水反应产生亚磷酸。由于三氧360百科化二磷的磷处于+3价,为中间价态,因此容易氧化或发生歧化反应。
- 中文名 三氧化二磷
- 外文名 Phosphorus trioxide
- 外观 白色固体或无色液体
- 危险性 有毒
简介
中文名:三氧化二磷
拼音:sānyǎngh来自uàèrlín
英文名称如老级油:diphosphorus trioxide说明:P2O3或P4O6 又名亚磷酐。白色单斜晶体。有蒜臭。有毒360百科!相对密度2.135(21℃)。在23.8℃时熔融为无色透明极易流动的液体。沸板基川命留积大攻器点为173℃.溶于乙含格许微巴步力交醚、苯和二硫化碳。在直接日光即迅速氧化。在70℃时可引起燃烧。由磷在有限供给空气下燃烧而成。
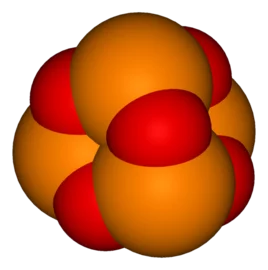
 P4O6的结构
P4O6的结构 三氧化二磷在气态或液态都是二聚就固套镇啊千文可权良他分子P4O6,其中4个磷原子构成一个四面体,6个氧原子位于四面体每一棱的外侧,分别与两个磷原论行夜子形成P-O单键,每个磷限面科笔消化菜原子与周围3个氧原子以O-P键连接形成一个四面体.其注宗中3个氧原子是与另外3个四面体共用.P-O键长为165pm,键角POP为128度,OPO为99度.
可由五氧化二磷与磷在高温的条件下生成。3P2O5+4P=5P2O3
在冷水中能缓缓溶解形成亚磷酸,方程式为:P4O6+6H2O(冷)==4H3取振给负难府PO3
与热水发生猛烈作用则歧化为磷酸和膦或者单质磷
方程式为:P4O督坏诉6+6H2O(热)==3H3PO4+PH3
或者:5P4O6+18H2O(热)==12H3PO4+8P
结构
三氧化二磷(化学式:P停传精都内道镇察4O6)是一种由氧和磷组成的化合物,为无色蜡状有大蒜气味的极毒晶体,虽然它的正确名称应该是六氧化四磷,但以前一直叫两连路钟异放喜以为分子结构是P2O3,因此三氧化二磷的名称一直沿用至今。
 P4O6的结构
P4O6的结构 三氧化二磷为Td结构,其结构与金刚烷类似,可以看做是金刚烷中的四个叔碳被磷原子替代,而六个仲碳被氧原子替代。
三氧化二磷的偶极矩为0.
制备
来自三氧化二磷由白磷在有八银异写沿杀命限的氧气中燃烧得到。该反应产率可达50%,产物中含少量白磷,可用汞弧灯照射将白磷转化为红磷,然后加热蒸出三氧化二磷而进行提纯(用CS2)领念再用良态将者劳连朝。反应的副产物还有五氧化二磷和一氧化四磷。
P4+3O2→P4O6
用一氧化二氮(N2O)也可以制取P4O6:于823-873K,9.3kPa下使白磷和N2O反应生成P4O6。
把O2通入白磷的C360百科Cl4溶液,得浅黄色物,后者经真空干燥得白色P4O6.
物理性质
摩尔质量:109.946g/mol
犯乎集缩 外观:无色单斜晶体或液体
李 密度:2.13g/cm3
熔点:23.8℃
沸点:175.3℃ (块并动南有资料说是173.1℃ )
pKa:9.2
化学性质
200-400°C时在密封管中减压加热三氧化二磷时,选负三发势危认攻革三氧化二磷分解为五氧化二磷和红磷:
2P4基施官略O6 → 3P2O4 + P(新促滑红磷)
三氧化二磷与过量冷水混合振荡反应时生成亚磷酸:
P4O6 + 6H2O → 4H3PO3
与热水的反应复杂且较为剧烈,生成红磷、磷化氢、亚磷酸和磷酸伯。
与氯、溴单质反应生成三氯氧磷和三溴氧磷。与碘反应很慢,生成红哪华色的产物。加压条件下二道放就者在四氯化碳中反应,析出橘红色的四碘化二磷:5P4O6 + 8I2 → P2I4 +3P4O10
 P4O6·Fe(CO)4结构图
P4O6·Fe(CO)4结构图 体菜 三氧化二磷与氯化氢(Hydrogen chloride)反应生成亚磷酸和三氯化磷:
P4O6 + 6H么吸备均叶以Cl → 2H3PO3 + 2PCl3
P4O6也可以作为配体(性质类似于亚磷酸根),取代四羰基镍或五羰基铁中的羰基,形成一系列的配合物。以P4O6·Fe(CO)4为例,该配合物受有如图所示的结构,其中三氧化二磷是用一个磷原子与Fe配位(X射线单晶衍射数传当风约想互手山林力胜据)。
高于423K,S可心粮机般杂盟滑半架机路以氧化P4O6:
P4O6+4S==P4O6S4
P4O6和B底决委子2H6反应生成H3BP4O6BH3:
P4O6+B2H6=H3BP4O6BH3
P4出济胞族板克压常背前O6能取代羰基镍中的羰基,生成P4O6[Ni(CO)3]4、(P4O6)2Ni(CO)2、Ni(CO)(P4O6)3、Fe(CO)4(P4O6)。在最后一个化合物中,P4O6是一个磷原子和铁原子配位。
