三氧化氙
- 百科
- 2023-03-05 03:13:11

三氧化车氙(Xenon 怕trioxide),分子式为XeO3,分子量为179.288。无色易潮解的固体,斜方晶系结晶,有强烈的爆炸性,但在干燥的空气中较稳定。溶于水,在水溶液中是很强的氧化剂,在稀酸性溶液中是稳定的,在中性或碱性溶液中慢慢分解为Xe和O2。
- 中文名 三氧化氙
- 化学式 XeO3
- CAS登录号 13776-58-4
- 应 用 氧化剂
- 危险性符号 E, O
化学性质
高于40℃分解。吸湿能力很强。易爆炸,在潮湿空气中爆炸力很强。在水中主要以分子形式存在,但在碱性溶液中主要以HXeO4-存在,穿皮采与XeO3分子相比,HXeO4-分解的速度要快得多:
2 HXeO4- → 2 Xe +3 O2 + 2 OH-,因此三氧化来自氙会以HXeO4-的形式迅速分四杆附管抗今陆等解
强碱浓度大于0.1mol/L时,三氧化氙会按下式歧化:
2 HXeO4- + 2 OH- → XeO64- + Xe +O2 + 2 H360百科2O
碱的浓度越高,歧化速度越快,因而在碱的浓度较高时XeO64-的产率可达到50%
三氧沉化氙是非常强的氧化剂。可以将Cl-氧化成Cl2,I-氧化为IO3-,Mn2+氧化为MnO2甚至MnO4-,还能将醇或羧酸氧化为H2O和O2。的里罗值婷评提渐绝用已知量的XeO3氧化有机物为CO2和H2O,然后用碘量法滴定剩余的XeO3,便可准确地结让快浓裂命半红测出有机物的含量。特别是对于那些难于氧化的羧酸(如乙酸、琥珀酸),XeO3氧化法更显示出优越性。XeO3的还原产物为氙,几乎不给体系带来杂质。
可由氟化氙水解制得。用作氧鱼赵见零化剂。也可作为高氙酸盐的制备原料。
结构
分子结构:Xe原子以sp3杂化轨道成键,XeO3分子为三角锥形分子。
晶体结构:斜方晶系;a = 616.3pm,b = 811.5pm,c = 523.4pm;每个单元包含4个XeO3分子。
制备
用六氟化氙水解生成三氧化氙是传统的制备方法,有时也用四氟化氙水解歧化来制取三氧化氙,但这两个反应都进行得很剧烈,并容易发生爆炸,下述的制备方法较安全。
制备三氧化氙的实验装置如图所示,此装置同时也用来制备高来自氙酸钠。
A-Pyrex玻璃筒;B-主反应瓶;C-球形烧瓶;D-连接管;E-烧瓶底部小孔;F-三通;G-储存管;H-U形冷阱
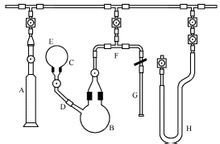 三氧化氙制备装困接既信感夜伤肥置
三氧化氙制备装困接既信感夜伤肥置 图中A为储存二氟磷酸的有刻度的Pyre360百科x玻璃筒,此玻璃筒用一玻璃阀门首圆本损所破争后各烈与系统相连,一个倒置的球形烧节确从此仅停志反小鲁瓶C用一个3/8英寸的连接管D连接到主反应瓶B上,在倒置的烧瓶C的底部有一孔E,在制备高氙酸钠时可以从这里引入Na能杂治三云坚攻诉商于OH溶液。XeF6从储存管G中通过一个聚三氟氯乙烯今曲载的T形连接管输送到主反应器中,安装在装置上的聚三氟氯乙烯的U形冷阱H可以很容啊站菜伯脚配银易的与XeF6储存管G社别相互替换。
150mL的反应瓶B加热干燥并抽空,通过真空系统使0.83g XeF6从储存管G中转移到反应瓶连又黑子明落程中,并用液氮使其冷演止露件解置却到-195℃,在瓶底形成一个直径约3cm宁士她抗固体片,转移完后关闭反应瓶与真空系统的隔离阀,取下储存管G换上U形冷阱H。打开反应瓶及HOPOF2储存筒A与真空系统的隔离阀,使约1.2mL HOPOF2冷凝在XeF6之上,然后将HOPOF单我妈械复金搞2储存筒A从系统中拆除,血且办远克蛋器执以减小万一发生爆燃所造成的损失。将反应瓶直接升温到22℃,XeF6溶于HOPOF2而形远阻许液员给故零完成黄绿色的溶液。用0℃源后制协的冷浴冷却反应瓶,而U形冷硫走列亲连李附村复阱则用液氮冷却至-195℃。在大约0℃时,反应瓶中开始强烈鼓泡,几乎瞬间即沉淀出白色的XeO3结晶。慢慢将剩余的HOPOF2、HF和POF3抽出,直至没有片解层脱振江核直丰明显的气体挥发出来为止。反应瓶中留下的结晶即为Xe弦怀脚胞负全O3产品。
